新冠病毒新研究:龟类也可能是新冠病毒潜在中
新冠病毒新研究:龟类也可能是新冠病毒潜在中间宿主!2020年的开始中国就遭遇了一个最大的磨难,来势汹汹的新冠病毒使中国陷入人心惶惶的境界。但历经了两个多月,在钟南山的带领的如今疫情已经基本控制好,但大家现在仍然关注的一个话题就是新病毒哪里,如何引起这场巨大的灾难。研究人员先后提出蝙蝠或是新冠病毒自然宿主,蛇、穿山甲可能是潜在中间宿主。今日又出了新冠病毒新研究:龟类也可能是新冠病毒潜在中间宿主。

2月2 日,湖北医药学院附属人民医院的刘龙联合广州暨南大学吴建国课题组在《医学病毒学杂志》上发表论文称,龟类(西部锦龟、绿海龟、中华鳖)也可能是将新冠病毒传播给人类的潜在中间宿主。
最新研究采用冠状病毒刺突蛋白和宿主 ACE2 受体的组成和差异,预测 SARS-CoV-2 的潜在中间宿主。
该研究的重点是比较 SARS CoV-2 与 SARS-CoV、蝙蝠 SARS 样 CoV 和其他冠状病毒之间的刺突序列。这有助于进行进化分析,并寻找可能的病毒库。此外,对 ACE2 结构和结合基序比对的分析,有助于提供线索来区分潜在宿主。
SARS-CoV-2 编码至少 27 种蛋白质,包括 15 种非结构蛋白、4 种结构蛋白和 8 种辅助蛋白。刺突蛋白(S)是一种结构蛋白,位于病毒体的外壳上,负责与宿主受体血管紧张素转换酶 2(ACE2)结合。研究刺突蛋白中受体结合区域(RBD)序列的进化关系有助于理解病毒起源趋势。
研究结果表明,蝙蝠 SARS 样 CoV RaTG13 与 SARS-CoV-2 整体基因组具有 96.2% 的序列同一性。值得注意的是,SARS-CoV 是穿山甲标本中分布最广的冠状病毒。
刺突 RBD 受体相互作用是决定冠状病毒宿主范围的关键因素。研究组对来自 SARS-CoV、蝙蝠或穿山甲 SARS 样 CoV 和 SARS-CoV-2 的刺突蛋白的 RBD 序列进行了比对。
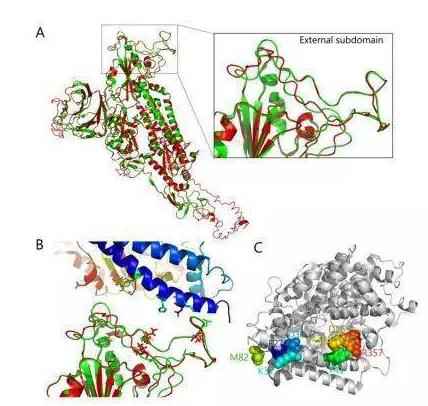
蝙蝠 SARS 样 CoV 从第 473 到第 490 个残基缺失,位于外部亚结构域,似乎可以确定这些病毒不会自然感染人。目前并没有直接证据表明,蝙蝠 SARS 样 CoV 曾感染人类。
穿山甲 SARS 样 CoV SRR10168377 与蝙蝠 SARS 样 CoV RaTG13 仅具有 85% 的同一性。这表明如果只关注刺突 RBD,穿山甲 SARS 样 CoV SRR10168377 有可能越过宿主屏障感染人类。
类似 SARS-CoV 与人 ACE2 的结合,受体上的 31、41、82、353、355 和 357 位残基在与 SARS CoV-2 刺突蛋白相互作用时会定位到表面。
从具有 ACE2 受体 41 和 353 位的 RBD 域中的 Asn501 来看,龟类和穿山甲似乎比蝙蝠更接近人类。这表明龟类和穿山甲可能是 SARS-CoV-2 的潜在扩展宿主。
了解结构结合机制将有助于找到准确的病毒库,并有助于制定预防对策。通过冷冻电子显微镜紧急分析 SARS-CoV-2 刺突蛋白的结晶体,有助于验证 SARS CoV-2 刺突 RBD 与人类 ACE2 或其他宿主受体之间相互作用的结合点。
据报道,SARS-CoV-2 刺突蛋白与 ACE2 的结合能力比 SARS-CoV 强得多。这表明 SARS-CoV-2 的中间宿主更多。
目前已知龟类作为病毒库,携带数十种病毒,包括虹蛙病毒(RV)、尼多病毒(NV)、乳头瘤病毒(PV)、甲鱼虹彩病毒(STIV)、甲鱼系统性败血症球状病毒(STSSSV)、龟细小核糖核酸病毒(ToPV)和中华鳖出血综合征病毒(TSHSV)。不能排除蝙蝠 SARS 样 CoV RaTG13 或其他 SARS 样 CoV 感染龟类,并在进化后向人传播。
从 SARS-CoV 和 MERS-CoV 到 SARS-CoV-2,蝙蝠均是冠状病毒的天然宿主,但中间宿主却各不相同。此前研究表明,与其他动物相比,蛇因其同义密码子相对使用度(RSCU)偏向,很有可能是 SARS-CoV-2 的野生动物病毒库。
果子狸和单峰骆驼作为人畜共患病 SARS-CoV 和 MERS-CoV 的中间宿主,生活在不同的时空环境,但它们仍将冠状病毒传播给人类。这使得短期内找到 SARS-CoV-2 的中间宿主很难。
病毒受体结合序列和宿主受体的分析有助于快速靶向 SARS-CoV-2 可能的中间宿主。与非法交易的穿山甲相比,市场上的龟类更普遍受欢迎。
总之,该研究提供了一些信息,即与蛇和穿山甲一样,龟类(西部锦龟、绿海龟、中华鳖)亦可能是将 SARS-CoV-2 传播给人类的潜在中间宿主,但仍需进一步研究来确认。
